中大新聞中心
中大研发新型多肽抑制剂 有望用以治疗柏金逊病
香港中文大学(中大)生命科学学院陈文博教授和李明名博士共同领导的研究团队,最近研发了一种新型多肽抑制剂,能够针对一种会破坏神经系统的蛋白聚集体,抑制其在脑部累积,或有助缓减多种神经退行性疾病,包括柏金逊病及路易氏体失智症的病情。这项研究已于《细胞化学生物学》(Cell Chemical Biology) 期刊发表。
柏金逊病是长者常见的神经系统疾病,可分为原发性和诱发性两类。大部分患有柏金逊病的长者都是原发性的,主要是由于脑内部分神经系统功能受损而引发,现阶段其明确成因未有医学实证。然而,近年有不同研究发现,柏金逊病患者和部分失智症患者的大脑神经细胞中,均存在大量α-突触核蛋白。它们积聚起来成为一些细小球状组织,称为路易氏体(Lewy bodies)。而这种蛋白聚集物具有神经毒性,能破坏神经细胞导致认知和运动功能衰退。
陈文博教授表示:「在柏金逊病、路易氏体失智症等神经退化性病人的脑部,大多会找到路易氏体及其主要成分α-突触核蛋白。我们相信若能够在患病初期有效抑制α-突触核蛋白的积聚,将可延缓病程恶化。」
新型多肽抑制剂的发现
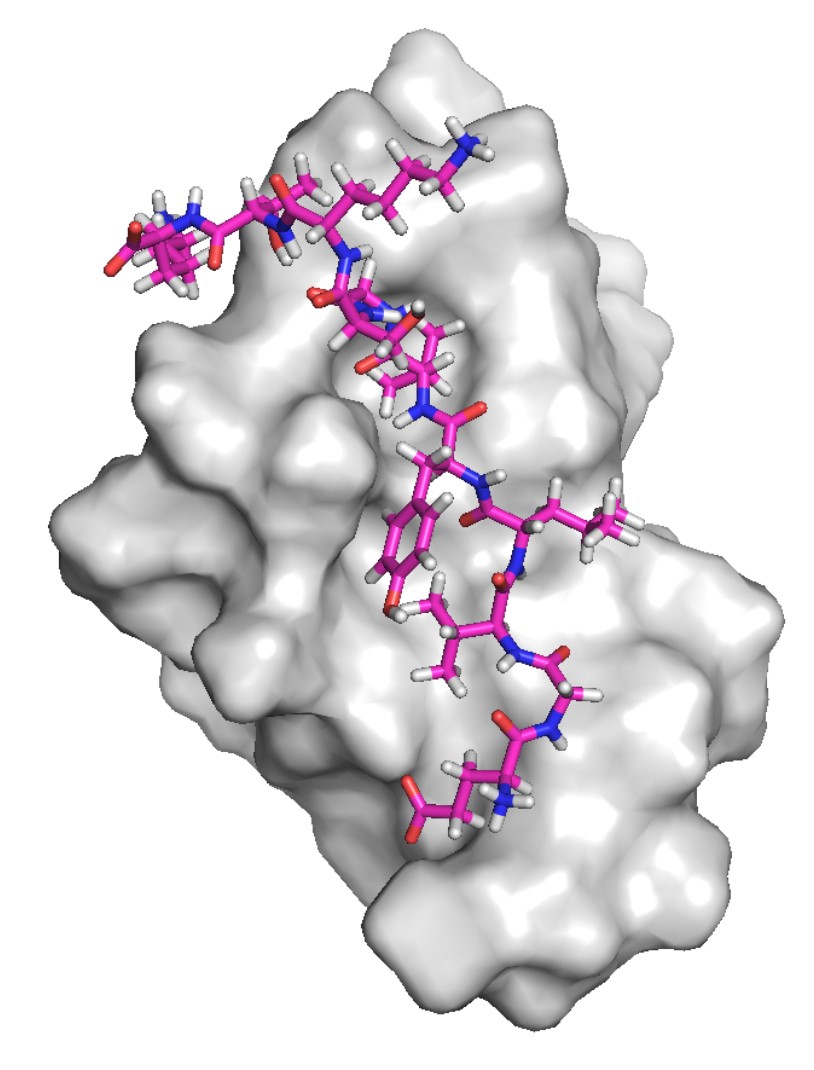
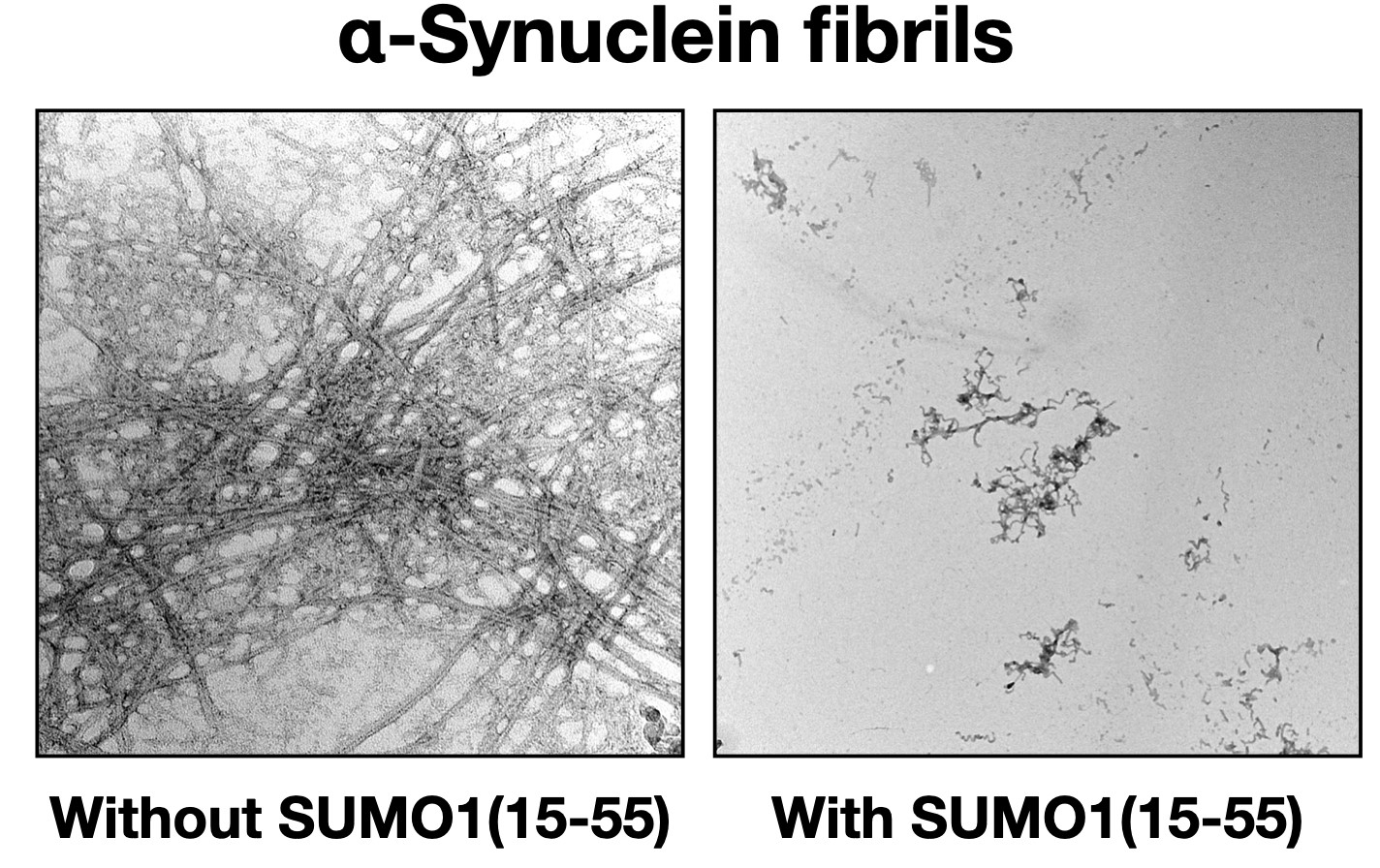
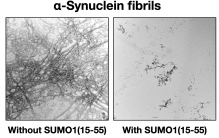
在研究团队的指导下,博士生梁兆辉在2015年意外发现一种特定的SUMO1蛋白变种体可以有效抑制α-突触核蛋白在脑神经积聚。研究团队随后花了五年时间,鉴定出SUMO1蛋白中的SUMO1(15-55) 结构片段能够与α-突触核蛋白结合,直接阻止其积聚。研究团队并阐述了其抑制作用的分子机理。
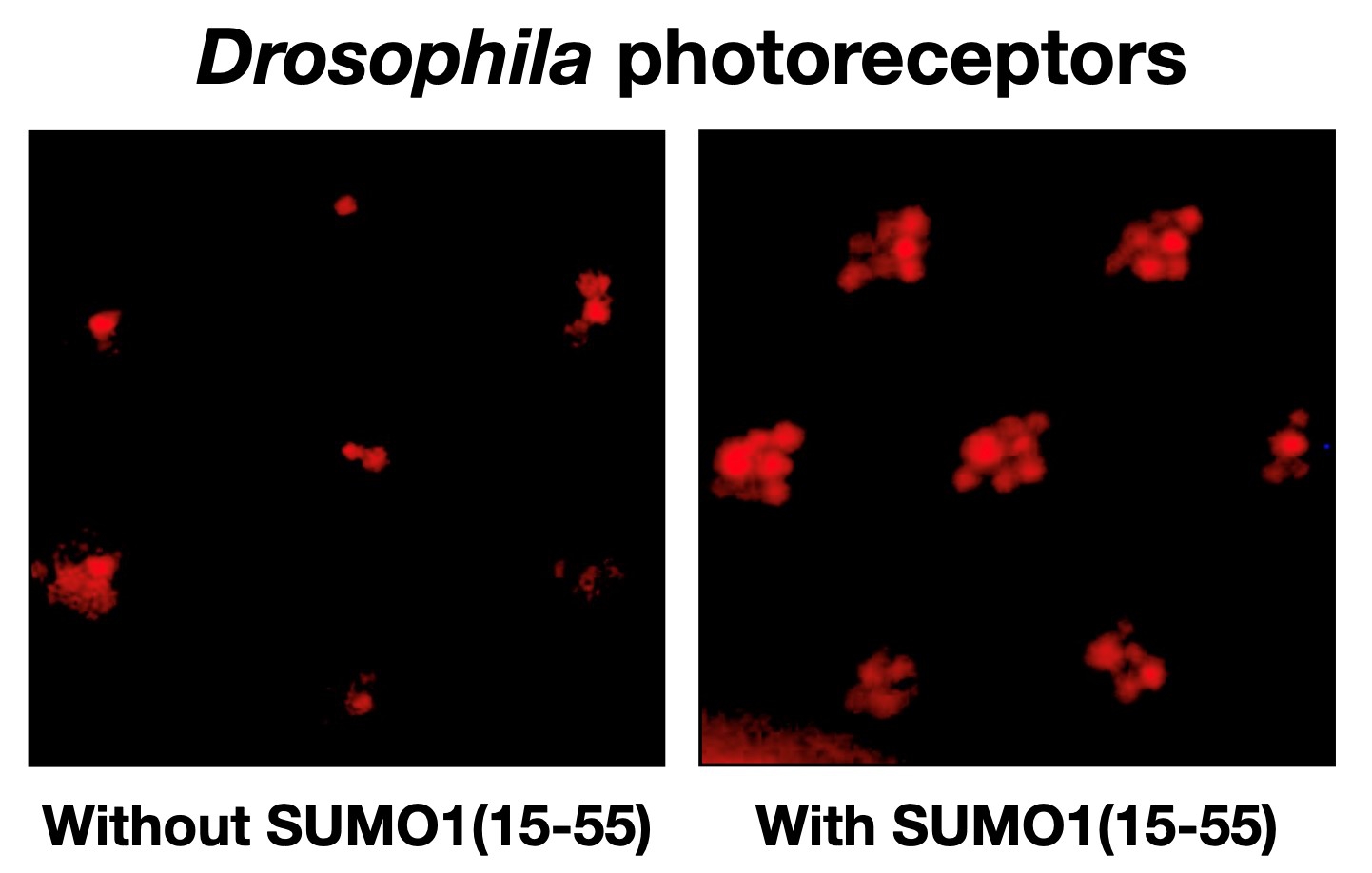
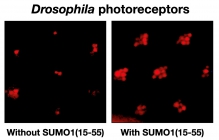
其后,团队与中大生命科学学院蔡永业脑神经科学中心陈浩然教授合作,将研究范围扩大,测试SUMO1(15-55) 对于有柏金逊病果蝇模型的神经保护作用。果蝇在幼虫期被注入SUMO1(15-55) 治疗后,减缓了成虫的神经退行性疾病的相关症状。研究结果显示该多肽抑制剂在治疗柏金逊病方面具有重大潜力。研究团队现在致力改善其生物稳定性、脑靶向能力和治疗功效,期望日后可供临床应用,改善患者病情。
此项目获得香港研究资助局卓越学科领域计划AoE/P-705/16、中大新型生物材料中心、生命科学学院,以及香港中文大学教员主要研究领域2转化生物医学研究奖励计划16/17的资金资助。
关于陈文博教授和李明名博士
陈文博教授目前是中大生命科学学院的教授,李明名博士是该学院的研究员。他们主要研究的题目包括化学生物学,以及蛋白质相关的生物化学,例如解析蛋白质结构、研发递送蛋白进入细胞的新技术。